Dạng bài tập xác định thành phần chất rắn sau phản ứng
Bài 1: Dẫn một luồng H2 đi qua 12 g CuO nung nóng. Sau phản ứng thu được 10,4 g chất rắn và một ít hơi H2O
a.Tính VH2 phản ứng
b. Tính Hpư
a.Tính VH2 phản ứng
b. Tính Hpư

Giải:
a. PTHH: H2 + CuO ® Cu + H2O
nCuO = 0,15 mol
Nếu CuO phản ứng hết thì theo PT: nCu = nCuO = 0,15 mol
mCuO = 0,5 . 64 = 9,6 g < 10,4 g
Vậy CuO phải dư, chất rắn sau phản ứng ngoài Cu còn có CuO dư
Gọi x là số mol CuO pư ® nCuO dư = 0,15-x
Theo PT: nCu = nCuO(pư) = x mol
Theo bài ra ta có: 64 x + 80 ( 0,15-x) = 10,4
Giải ra ta được x = 0,1 mol
VH2 pư = 0,1 . 22,4 = 2,24 lit
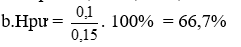
Bài 2: Cho a g Zn tan hết trong dd HCl thu được V(l) H2 (đktc). Dẫn V(l) H2 đi qua ống đựng 80 g CuO nung nóng. Sau một thời gian còn lại 72,32 g chất rắn và chỉ có 80% H2 tham gia phản ứng. Tính V? a?
Giải:
nCuO = 1 mol
Zn + 2HCl ® ZnCl2 + H2 (1)
H2 + CuO ® Cu + H2O (2)
x x x
Gọi x là số mol CuO pư ® nCuO dư = 1-x
Theo PT: nCu = nCuO = x mol
Theo bài ra ta có: 64 x + 80 ( 1-x) = 72,32
Giải ra ta được x = 0,48
Theo PT: nH2(pư) = x = 0,48 mol

Bài 3: Nhiệt phân 9,4 g Cu(NO3)2 theo phương trình
2Cu(NO3)2 ® 2CuO + 4NO2 + O2
Sau một thời gian thu được 7,24 g chất rắn
Tính Hpư nhiệt phân
Giải:

Bài 4: Cho sơ đồ phản ứng
H2 + Fe2O3 ® Fe + H2O
a.Lập PTHH
b. Hãy điền vào những ô trống số mol chất phản ứng và sản phẩm có ở những thời điểm khác nhau. Biết số mol H2 và Fe2O3 ban đầu được lấy đúng tỷ lệ theo PTHH
Bài 5: Cho vào bình kín CuO và khí CO dư đốt nóng, phản ứng xẩy ra theo PT
CuO + CO ® Cu + CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
Kẻ lại bảng trên vào bài làm và điền các giá trị thích hơp vào ô trống
Giải:
Bài 6:
Cho vào bình kín Fe2O3 và khí CO dư đốt nóng, phản ứng xẩy ra theo PT
Fe2O3 + 3CO ® 2Fe +3 CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
Kẻ lại bảng trên vào bài làm và điền các giá trị thích hơp vào ô trống
Giải:
Bài 7: Cho vào bình kín Fe3O4 và khí CO dư đốt nóng, phản ứng xẩy ra theo PT
Fe3O4 + 4CO ® 3Fe +4CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
Giải:
a. PTHH: H2 + CuO ® Cu + H2O
nCuO = 0,15 mol
Nếu CuO phản ứng hết thì theo PT: nCu = nCuO = 0,15 mol
mCuO = 0,5 . 64 = 9,6 g < 10,4 g
Vậy CuO phải dư, chất rắn sau phản ứng ngoài Cu còn có CuO dư
Gọi x là số mol CuO pư ® nCuO dư = 0,15-x
Theo PT: nCu = nCuO(pư) = x mol
Theo bài ra ta có: 64 x + 80 ( 0,15-x) = 10,4
Giải ra ta được x = 0,1 mol
VH2 pư = 0,1 . 22,4 = 2,24 lit
Bài 2: Cho a g Zn tan hết trong dd HCl thu được V(l) H2 (đktc). Dẫn V(l) H2 đi qua ống đựng 80 g CuO nung nóng. Sau một thời gian còn lại 72,32 g chất rắn và chỉ có 80% H2 tham gia phản ứng. Tính V? a?
Giải:
nCuO = 1 mol
Zn + 2HCl ® ZnCl2 + H2 (1)
H2 + CuO ® Cu + H2O (2)
x x x
Gọi x là số mol CuO pư ® nCuO dư = 1-x
Theo PT: nCu = nCuO = x mol
Theo bài ra ta có: 64 x + 80 ( 1-x) = 72,32
Giải ra ta được x = 0,48
Theo PT: nH2(pư) = x = 0,48 mol

Bài 3: Nhiệt phân 9,4 g Cu(NO3)2 theo phương trình
2Cu(NO3)2 ® 2CuO + 4NO2 + O2
Sau một thời gian thu được 7,24 g chất rắn
Tính Hpư nhiệt phân
Giải:

Bài 4: Cho sơ đồ phản ứng
H2 + Fe2O3 ® Fe + H2O
a.Lập PTHH
b. Hãy điền vào những ô trống số mol chất phản ứng và sản phẩm có ở những thời điểm khác nhau. Biết số mol H2 và Fe2O3 ban đầu được lấy đúng tỷ lệ theo PTHH
| Các thời điểm | Số mol | |||
| Chất tham gia | Sản phẩm | |||
| H2 | Fe2O3 | Fe | H2O | |
| Ban đầu | 30 | 10 | 0 | 0 |
| T1 | 24 | |||
| T2 | 7 | |||
| T3 | 16 | |||
| T4 | 27 | |||
| T5 | 30 | |||
Bài 5: Cho vào bình kín CuO và khí CO dư đốt nóng, phản ứng xẩy ra theo PT
CuO + CO ® Cu + CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mCuO (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 24 | |||
| T1 | 22,4 | |||
| T2 | 18 | |||
| Kết thúc tk | 4,48 | |||
Kẻ lại bảng trên vào bài làm và điền các giá trị thích hơp vào ô trống
Giải:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mCuO (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 24 | 11,2 | 24 | 14 |
| T1 | 16 | 8,96 | 22,4 | 15,6 |
| T2 | 4 | 5,6 | 20 | 18 |
| Kết thúc tk | 0 | 4,48 | 19,2 | 18,8 |
Bài 6:
Cho vào bình kín Fe2O3 và khí CO dư đốt nóng, phản ứng xẩy ra theo PT
Fe2O3 + 3CO ® 2Fe +3 CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mFe2O3 (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 32 | |||
| T1 | 29,6 | |||
| T2 | 18 | |||
| Kết thúc tk | 6,72 | |||
Giải:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mFe2O3 (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 32 | 20,16 | 32 | 14 |
| T1 | 24 | 16,8 | 29,6 | 15,3 |
| T2 | 8 | 10,08 | 24,8 | 18 |
| Kết thúc tk | 0 | 6,72 | 22,4 | 19,3 |
Fe3O4 + 4CO ® 3Fe +4CO2
Lượng các chất trong bình tại một số thời điểm cho trong bảng sau:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mFe3O4 (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 58 | |||
| T1 | 54,8 | |||
| T2 | 18 | |||
| Kết thúc tk | 4,48 | |||
Giải:
| Thời điểm | Lượng các chất trong bình | dhh/H2 | ||
| mFe3O4 (g) | VCO (l) | m (chất rắn) | ||
| Ban đầu t0 | 58 | 26,88 | 58 | 14 |
| T1 | 46,4 | 22,4 | 54,8 | 15,3 |
| T2 | 23,2 | 13,44 | 48,4 | 18 |
| Kết thúc tk | 4,48 | |||
Ý kiến bạn đọc
Bạn cần đăng nhập với tư cách là Thành viên chính thức để có thể bình luận
Những tin mới hơn
Những tin cũ hơn
global video
-
-
 Hướng dẫn giải bài tập về vận...
hướng dẫn ôn tập và giải các bài tập về
Hướng dẫn giải bài tập về vận...
hướng dẫn ôn tập và giải các bài tập về
-
 Hướng dẫn giải bài tập về công...
hướng dẫn ôn tập và giải các bài tập về công cơ học
Hướng dẫn giải bài tập về công...
hướng dẫn ôn tập và giải các bài tập về công cơ học
-
 Hướng dẫn giải bài tập về lực...
Hướng dẫn giải bài tập về
Hướng dẫn giải bài tập về lực...
Hướng dẫn giải bài tập về
Thăm dò ý kiến
Tin xem nhiều
-
 Bài tập về thấu kính hội tụ
Bài tập về thấu kính hội tụ
-
 DẠNG TOÁN HỖN HỢP TRONG HÓA HỌC
DẠNG TOÁN HỖN HỢP TRONG HÓA HỌC
-
 ĐỀ THI CHỌN ĐỘI TUYỂN HỌC SINH GIỎI LỚP 9 MÔN GDCD
ĐỀ THI CHỌN ĐỘI TUYỂN HỌC SINH GIỎI LỚP 9 MÔN GDCD
-
 ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9 MÔN NGỮ VĂN
ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9 MÔN NGỮ VĂN
-
 Bài tập về thấu kính phân kỳ
Bài tập về thấu kính phân kỳ
-
 Dạng bài tập về Đoạn mạch nối tiếp
Dạng bài tập về Đoạn mạch nối tiếp
-
 Cách mạng tháng tám 1945: Thời cơ, diễn biến, ý nghĩa lịch sử và bài học kinh nghiệm của cách mạng tháng tám 1945
Cách mạng tháng tám 1945: Thời cơ, diễn biến, ý nghĩa lịch sử và bài học kinh nghiệm của cách mạng tháng tám 1945
-
 Dạng bài tập đoạn mạch song song
Dạng bài tập đoạn mạch song song
-
 CUỘC CÁCH MẠNG KHOA HỌC KĨ THUẬT LẦN THỨ HAI
CUỘC CÁCH MẠNG KHOA HỌC KĨ THUẬT LẦN THỨ HAI
-
 TRỢ TỪ – THÁN TỪ – TÌNH THÁI TỪ
TRỢ TỪ – THÁN TỪ – TÌNH THÁI TỪ
Thống kê
- Đang truy cập52
- Hôm nay14,783
- Tháng hiện tại263,164
- Tổng lượt truy cập20,425,182
Tài liệu mới
- chuyên đề Phương trình... - 18/04/2022
- Phương trình chứa ấn ở... - 28/02/2020
- Các dạng bài tập phương... - 28/02/2020
- Giáo án dạy thêm toán 6 - 27/02/2020
- Chuyên đề bồi dưỡng học... - 27/02/2020
