SỬ DỤNG PHƯƠNG PHÁP ION - ELECTRON
Phương pháp này sử dụng để giải nhanh nhiều bài toán khó mà nếu giải bằng phương pháp thông thường thì rất mất thời gian thậm trí bế tắc. Lưu ý cách tính nhanh số mol anion tạo muối và số mol axit tham gia phản ứng trong phản ứng oxi - hóa khử.

a) Axit H2SO4 đặc
Không phụ thuộc vào bản chất và số lượng các kim loại ta luôn có các bán phản ứng khử:

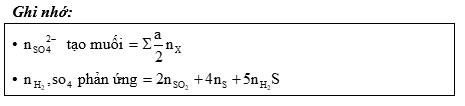
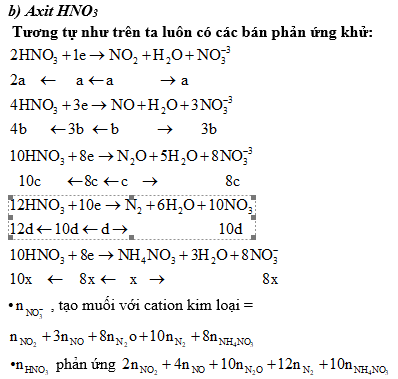
Chú ý: - Các công thức trên không thể áp dụng nếu chất khử ban đầu không phải là kim loại.
- Nếu hỗn hợp ban đầu không hoàn toàn là kim loại thì ta nên quy hỗn hợp về các nguyên tố rồi dựa vào phương trình ion - electron của bán phản ứng oxi hoá và bán phản ứng khử để giải.
Ví dụ 1: Cho 29 gam hỗn hợp gồm Al, Cu và Ag tác dụng vừa đủ với dịch HNO3 1,5M, thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỉ khối của X so với H2 là 16,4. Giá trị của m là
A. 98,20 B. 97,20 C. 98,75 D. 91,00

Ví dụ 2: Hòa tan hoàn toàn 0,1 mol FeS2 trong 200 ml dung dịch HNO3 4M, sản phẩm thu được gồm dung dịch X và một chất khí thoát ra. Dung dịch X có thể hòa tan tối đa m gam Cu. Biết trong các quá trình trên, sản phẩm khử duy nhất của N+5 đều là NO. Giá trị của m là
A. 12,8 B. 6,4 C.9,6 D. 3,2
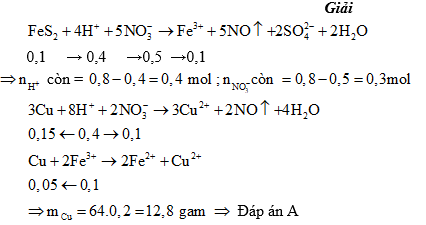
Ví dụ 3: Cho 19,2 gam Cu vào 500 ml dung dịch NaNO3 1M, sau đó thêm vào 500 ml dung dịch HCl 2M, Kết thúc phản ứng thu được dung dịch X và khí NO duy nhất, phải thêm bao nhiêu ml dung dịch NaOH 1M vào X để kết tủa hết ion Cu2+
A. 120 B. 400 C. 600 D. 800

Ví dụ 4: Chia 23,0 gam hỗn hợp M gồm Al, Cu và Mg thành hai phần bằng nhau.
Phần 1 tác dụng với dung dịch HCl dư, sinh ra 5,6 lít H2 (đktc). Hoà tan hết phần 2 trong 120 gam dung dịch HNO3 63% đun nóng, kết thúc phản ứng thu được dung dịch X và 8,96 lít (đktc) hỗn hợp hai khí NO, NO2 có tỉ khối so với H2 là 20. X tác dụng với dung dịch NaOH đun nóng, không có khí mùi khai thoát ra.
a) Tính phần trăm khối lượng mỗi chất trong M.
b) Tính nồng độ phần trăm các chất trong X. Coi nước bay hơi không đáng kể trong quá trình phản ứng.
Giải
a)
• Phần 1: Cu không phản ứng
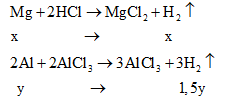



Ví dụ 5: Cho 42 gam hỗn hợp X gồm Fe, Cu vào 1 lít dung dịch HNO3 1M, kết thúc phản ứng thu được dung dịch Y, V1 lít khí NO (sản phẩm khử duy nhất, đktc) và còn lại m gam Cu không tan. Nhỏ 800 ml dung dịch HCl 1M vào thì kim loại vừa tan hết và thu thêm V2 lít khí NO nữa.
a) Tính V1, V2 và m.
b) Tính phần trăm khối lượng các kim loại trong X.
Giải

Vì Cu còn dư nên Fe chỉ bị oxi hoá lên Fe2+ . Khi nhỏ tiếp HCl vào hỗn hợp thực chất là thêm H+ thì do tính khử của Fe2+ yếu hơn Cu nên Cu phản ứng hết. Khi Cu vừa tan hết thì ngừng thêm H+ nên Fe2+ chưa bị oxi hoá thành Fe3+


Không phụ thuộc vào bản chất và số lượng các kim loại ta luôn có các bán phản ứng khử:

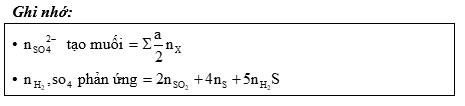
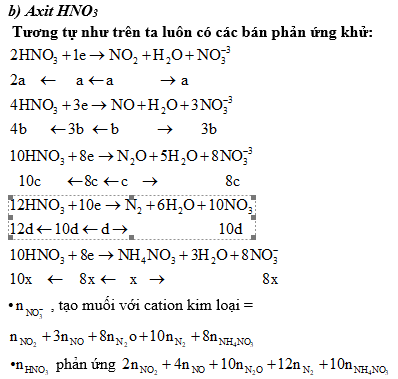
Chú ý: - Các công thức trên không thể áp dụng nếu chất khử ban đầu không phải là kim loại.
- Nếu hỗn hợp ban đầu không hoàn toàn là kim loại thì ta nên quy hỗn hợp về các nguyên tố rồi dựa vào phương trình ion - electron của bán phản ứng oxi hoá và bán phản ứng khử để giải.
Ví dụ 1: Cho 29 gam hỗn hợp gồm Al, Cu và Ag tác dụng vừa đủ với dịch HNO3 1,5M, thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỉ khối của X so với H2 là 16,4. Giá trị của m là
A. 98,20 B. 97,20 C. 98,75 D. 91,00

Ví dụ 2: Hòa tan hoàn toàn 0,1 mol FeS2 trong 200 ml dung dịch HNO3 4M, sản phẩm thu được gồm dung dịch X và một chất khí thoát ra. Dung dịch X có thể hòa tan tối đa m gam Cu. Biết trong các quá trình trên, sản phẩm khử duy nhất của N+5 đều là NO. Giá trị của m là
A. 12,8 B. 6,4 C.9,6 D. 3,2
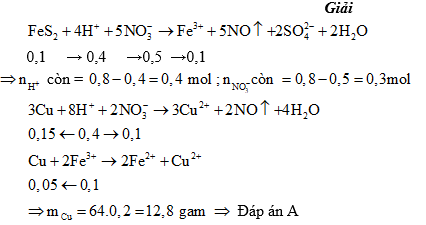
Ví dụ 3: Cho 19,2 gam Cu vào 500 ml dung dịch NaNO3 1M, sau đó thêm vào 500 ml dung dịch HCl 2M, Kết thúc phản ứng thu được dung dịch X và khí NO duy nhất, phải thêm bao nhiêu ml dung dịch NaOH 1M vào X để kết tủa hết ion Cu2+
A. 120 B. 400 C. 600 D. 800

Ví dụ 4: Chia 23,0 gam hỗn hợp M gồm Al, Cu và Mg thành hai phần bằng nhau.
Phần 1 tác dụng với dung dịch HCl dư, sinh ra 5,6 lít H2 (đktc). Hoà tan hết phần 2 trong 120 gam dung dịch HNO3 63% đun nóng, kết thúc phản ứng thu được dung dịch X và 8,96 lít (đktc) hỗn hợp hai khí NO, NO2 có tỉ khối so với H2 là 20. X tác dụng với dung dịch NaOH đun nóng, không có khí mùi khai thoát ra.
a) Tính phần trăm khối lượng mỗi chất trong M.
b) Tính nồng độ phần trăm các chất trong X. Coi nước bay hơi không đáng kể trong quá trình phản ứng.
Giải
a)
• Phần 1: Cu không phản ứng
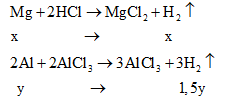



Ví dụ 5: Cho 42 gam hỗn hợp X gồm Fe, Cu vào 1 lít dung dịch HNO3 1M, kết thúc phản ứng thu được dung dịch Y, V1 lít khí NO (sản phẩm khử duy nhất, đktc) và còn lại m gam Cu không tan. Nhỏ 800 ml dung dịch HCl 1M vào thì kim loại vừa tan hết và thu thêm V2 lít khí NO nữa.
a) Tính V1, V2 và m.
b) Tính phần trăm khối lượng các kim loại trong X.
Giải

Vì Cu còn dư nên Fe chỉ bị oxi hoá lên Fe2+ . Khi nhỏ tiếp HCl vào hỗn hợp thực chất là thêm H+ thì do tính khử của Fe2+ yếu hơn Cu nên Cu phản ứng hết. Khi Cu vừa tan hết thì ngừng thêm H+ nên Fe2+ chưa bị oxi hoá thành Fe3+


Ý kiến bạn đọc
Bạn cần đăng nhập với tư cách là Thành viên chính thức để có thể bình luận
Những tin mới hơn
Những tin cũ hơn
global video
-
-
 Hướng dẫn giải bài tập về vận...
hướng dẫn ôn tập và giải các bài tập về
Hướng dẫn giải bài tập về vận...
hướng dẫn ôn tập và giải các bài tập về
-
 Hướng dẫn giải bài tập về công...
hướng dẫn ôn tập và giải các bài tập về công cơ học
Hướng dẫn giải bài tập về công...
hướng dẫn ôn tập và giải các bài tập về công cơ học
-
 Hướng dẫn giải bài tập về lực...
Hướng dẫn giải bài tập về
Hướng dẫn giải bài tập về lực...
Hướng dẫn giải bài tập về
Thăm dò ý kiến
Tin xem nhiều
-
 Bài tập về thấu kính hội tụ
Bài tập về thấu kính hội tụ
-
 DẠNG TOÁN HỖN HỢP TRONG HÓA HỌC
DẠNG TOÁN HỖN HỢP TRONG HÓA HỌC
-
 ĐỀ THI CHỌN ĐỘI TUYỂN HỌC SINH GIỎI LỚP 9 MÔN GDCD
ĐỀ THI CHỌN ĐỘI TUYỂN HỌC SINH GIỎI LỚP 9 MÔN GDCD
-
 ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9 MÔN NGỮ VĂN
ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9 MÔN NGỮ VĂN
-
 Bài tập về thấu kính phân kỳ
Bài tập về thấu kính phân kỳ
-
 Dạng bài tập về Đoạn mạch nối tiếp
Dạng bài tập về Đoạn mạch nối tiếp
-
 Cách mạng tháng tám 1945: Thời cơ, diễn biến, ý nghĩa lịch sử và bài học kinh nghiệm của cách mạng tháng tám 1945
Cách mạng tháng tám 1945: Thời cơ, diễn biến, ý nghĩa lịch sử và bài học kinh nghiệm của cách mạng tháng tám 1945
-
 Dạng bài tập đoạn mạch song song
Dạng bài tập đoạn mạch song song
-
 CUỘC CÁCH MẠNG KHOA HỌC KĨ THUẬT LẦN THỨ HAI
CUỘC CÁCH MẠNG KHOA HỌC KĨ THUẬT LẦN THỨ HAI
-
 TRỢ TỪ – THÁN TỪ – TÌNH THÁI TỪ
TRỢ TỪ – THÁN TỪ – TÌNH THÁI TỪ
Thống kê
- Đang truy cập74
- Hôm nay12,072
- Tháng hiện tại301,566
- Tổng lượt truy cập20,463,584
Tài liệu mới
- chuyên đề Phương trình... - 18/04/2022
- Phương trình chứa ấn ở... - 28/02/2020
- Các dạng bài tập phương... - 28/02/2020
- Giáo án dạy thêm toán 6 - 27/02/2020
- Chuyên đề bồi dưỡng học... - 27/02/2020
